Vi startar en egen tråd för den här också. Nytt läkemedelsbolag till First North-listan genom en duonotering. Ett trevligt tillskott till Helsingforsbörsen ![]()
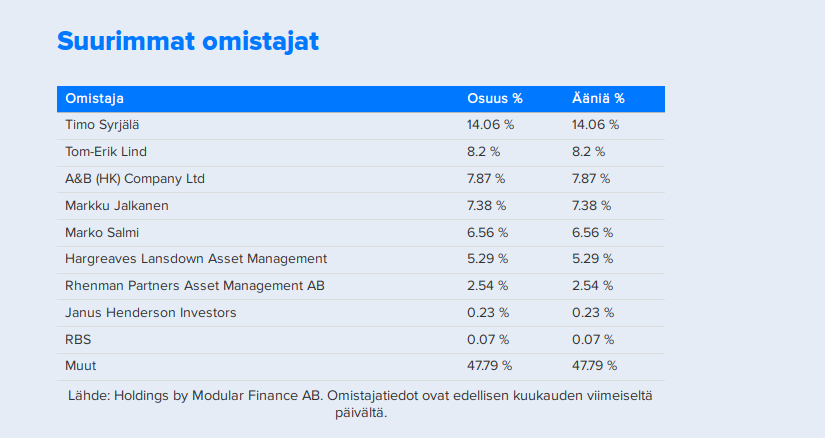
Bolagssidan visar nu de 10 största ägarna: Faron Pharmaceuticals - osake - Inderes
Lottokuponger ![]()
Endast JNJ finns i portföljen. Annars går vi rent via ETF om det av någon anledning är nödvändigt att investera i branschen.
Men den modige får kakan (någon annan än undertecknad).
Jag vill verkligen inte vara en negativ nördig igen, men när man först noterar sig utomlands, sedan söker finansiering från en begränsad grupp investerare, och sedan söker sig till en grupp privata investerare, och dessutom från Finland, då luktar det alltid lite skit för mig ![]()
Vi försöker få VD:n att ställa upp på en intervju med oss. ![]()
Söks dock tilläggsfinansiering från Finland? Är inte detta bara en parallell notering för synlighet och liknande?
Pengarna räcker till första kvartalet. Utan försäljning och med löpande kostnader töms kassan snabbt.
Faron har sin finansiering i ordning för de kommande 12 månaderna efter finansieringsrundan i november, vilket också är en förutsättning för notering på First North. Ytterligare finansiering söktes inte i samband med noteringen på First North och kommer tydligen inte att sökas inom en snar framtid, eftersom Faron i den föregående finansieringsrundan förband sig att inte genomföra aktieemissioner under minst de kommande 6 månaderna.
All information finns i AIM:s börsmeddelanden. Dessa meddelanden visar också att Faron förhandlar om licensavtal med flera partners gällande immuncancerläkemedlet Clevegen, och förhandlingarna är avsedda att slutföras under de kommande månaderna. Denna typ av avtal är vanligtvis betydande, så företaget har en enorm potential om de lyckas få till licensavtalen.
Det lönar sig att bekanta sig ordentligt med företaget innan man börjar kommentera. DYOR.
Mitt misstag. Jag märkte inte det meddelandet, utan sa bara vad som nämndes i den senaste delårsrapporten. Det vill säga, pengarna tar slut och mer behövs. Bra dock om saken är omhändertagen för en stund.
Utvecklingsarbete är dock dyrt och blir dyrare utan säkerhet att få något säljbart på marknaden. Dessa företag har knappt funnits i Finland och saken är säkert ny för de flesta på forumet. Risken att förlora en betydande del av kapitalet är mycket sannolik i dessa företag och knappast någon har expertis att bedöma om medicinen kommer ut på marknaden när fasstudierna fortskrider.
Ur detta perspektiv är det viktigt att bredda finansieringsbasen. Misstankar väcks dock hos mig när OMXH (Helsingforsbörsen) hoppas över och en notering söks även här i ett senare skede. En sund misstanke är alltid bra.
Visst var det ursprungliga syftet att lista sig utomlands och nå framgång med Traumakine, men när det misslyckades i Fas 3 för den primära indikationen, har man nu behövt utforska andra möjligheter. Detta är mest en magkänsla, men om Traumakine hade lyckats, tvivlar jag på att man skulle ha strävat efter en parallell notering här.
Vad tycker forummedlemmarna om dagens MATINS-uppdatering? Jag tolkar den åtminstone som ett positivt budskap gällande den studien.
{“content”:“Jag såg den här nyheten idag. Detta är väl en fortsättning på produktionsuppdateringen som tillkännagavs i oktober? \n404 HTML Template”}
Jag har börjat undersöka företaget Farnon Pharmaceuticals lite mer. Hittills har jag investerat i företag vars ekonomiska rapporter tydligt visar mer intäkter än utgifter, så detta skulle vara en total motsats. Dessutom kan det snarare handla om välgörenhet än en investering, men det skulle vara en utmaning att kliva helt utanför mitt eget expertisområde ![]()
![]()
![]()
Finns det några rationella skäl för att investera i ett sådant läkemedelsföretag?
Jag hittade en intressant blogg som handlar om att investera i läkemedelsföretag. Jag har inte hunnit läsa den ordentligt än, men jag tänkte dela med mig av ett par saker till andra ![]()
Lääkärin resepti: helmikuuta 2013
Jag hittade också ett par videor om Faron på YouTube som inte fanns på företagets egna sidor.
Färskt från pressen ![]()
![]()
![]()
{“content”:“Jag tog en liten position i detta idag. Det har potential att stiga mycket och snabbt. Jag vet inte hur förnuftigt det är. Förhoppningsvis går pengarna till ett gott ändamål om de försvinner.”,“target_locale”:“sv”}
{“content”:“Lite samma tankar här. Jag läste i någon investeringsbok eller hörde via en podcast att man inte utvecklas inom investeringar om man aldrig utmanar sig själv utanför sin bekvämlighetszon. Jag gillar att fördjupa mig i saker så om man satsar lite pengar på detta med en “välgörenhets”-princip så får man åtminstone studera något okänt igen.\n\nFaron har en aktiv grupp supportrar här. De förväntar sig ivrigt att mer goda nyheter ska komma.\nhttps://www.lse.co.uk/ShareChat.asp?ShareTicker=FARN&share=Faron-Pharma”}
https://m.fi.investing.com/equities/faron-pharmaceuticals-Oy Därifrån tittar jag ibland på kursen. Där ser man också att det för närvarande finns en stark köprekommendation.
Faron har också förnyat sin webbplats
Jag köper en liten position imorgon så att intresset hålls uppe bättre.
Vad tycker ni om Farons nya webbplats?
Jag gillade att avsnittet Pipeline nu mycket tydligt visar all pågående forskning och i vilket skede den befinner sig.
Ny RNS-bulletin från Faron idag. Jag har inte sett den på hemsidan än så jag kopierar den här. Den korta tid jag har följt Faron brukar RNS-bulletinerna skapa spänning och aktiekursen går fint uppåt om nyheten är positiv. Om jag förstår rätt testas nu läkemedlet på en eventuell ny målgrupp?
Faron Pharmaceuticals Oy
(“Faron” eller “Bolaget”)
MATINS UPPFÖLJNING AV STUDIEN
Äggstockscancer vald som andra expansionskohort
Företagsmeddelande, 27 januari 2020 kl. 9.00 (EET)
Insiderinformation
ÅBO – FINLAND – Faron Pharmaceuticals Oy (AIM: FARN, First North: FARON), det kliniska bioteknikföretaget, meddelar idag att den andra expansionskohorten i dess fas I/II MATINS kliniska studie som undersöker säkerheten och effektiviteten av Clevegen kommer att omfatta patienter med äggstockscancer.
Den pågående fas I/II MATINS kliniska studien undersöker tolerabiliteten, säkerheten och effektiviteten av Clevegen, Farons helägda nya precisionscancerimmunterapi som riktar sig mot Clever-1 positiva tumörassocierade makrofager (TAM), i utvalda metastaserade eller inoperabla solida tumörer.
Initieringen av denna andra expansionskohort följer godkännandet från MATINS-studiens datakontrollkommitté tidigare denna månad att initiera studiens första expansionskohort hos patienter som lider av sent stadium av kolorektal cancer (CRC). Äggstockscancer är en tumörtyp som är känd för att hysa ett betydande antal Clever-1 positiva tumörassocierade makrofager (TAM). Den utgör ett stort ometet medicinskt behov med få tillgängliga behandlingar för patienter. Stor transkriptanalys av äggstockstumörer indikerar betydande utfalls skillnader mellan patienter med antingen hög eller låg Clever-1-uttryck. Patienter med högt Clever-1-uttryck har korta livslängder under nuvarande behandlingsalternativ.
Dr. Markku Jalkanen, Farons VD, sade: “Data som hittills samlats in i MATINS-studien är mycket uppmuntrande, med Clevegen som etablerar sig som en potentiell immunterapi som kan nedreglera en rad stora hämmande immunkontrollpunkter (PD-1, PD-L1, CTLA-4) över flera cancerformer. Initieringen av denna ytterligare expansionskohort signalerar vårt engagemang att snabbt driva utvecklingen av Clevegen hos patienter med begränsade effektiva behandlingsalternativ.”
Dr. Tyler Curiel, professor och The Daisy M. Skinner President’s Chair in Cancer Immunology Research, UT Health San Antonio, och MATINS-studiens prövare och huvudprövare för USA, sade: “Äggstockscancer är förödande och det finns fortfarande ett enormt behov av nya behandlingar. Att expandera MATINS-studien till att inkludera patienter med äggstockscancer kommer att hjälpa oss att förstå denna nya potentiella immunterapi i en patientgrupp där vi desperat behöver förbättra resultaten. Vi är mycket glada över att delta i MATINS-studien och att starta rekrytering i USA.”
Befintliga MATINS-studieplatser i Europa rekryterar för närvarande för den första expansionskohorten hos sent stadium av CRC-patienter och denna andra kohort, med totalt 10 patienter med äggstockscancer, förväntas följa under de kommande veckorna. Med god tolerabilitet och inga dosbegränsande toxicitetssignaler etablerade över alla dosnivåer som hittills utforskats i MATINS-studien, är doseringen för denna ytterligare kohort sannolikt högre (t.ex. 1 mg/kg) än för den första CRC-kohorten. MATINS-studieplatser i USA förväntas börja öppna inom kort.
Primärt avsedd att undersöka säkerhet och tolerabilitet, har den avslutade del I av MATINS-studien redan visat att Clevegen-administrering främjade immunaktivering hos alla doserade patienter hittills. Detta skulle potentiellt göra Clevegen till ett nytt och effektivt makrofagimmunkontrollpunktsläkemedel för cancerpatienter, som ofta lider av undertryckt immunkapacitet för tumöreliminering. Tidigare meddelade data indikerar också att Clevegen kan nedreglera en rad stora hämmande immunkontrollpunkter, som nuvarande immuno-onkologiska terapier syftar till att undertrycka.
Detta meddelande innehåller insiderinformation i enlighet med artikel 7 i förordning (EU) nr 596/2014 (“MAR”).
För mer information kontakta:
Faron Pharmaceuticals Oy
Dr Markku Jalkanen, verkställande direktör
Panmure Gordon (UK) Limited, Nomad och mäklare
Emma Earl, Freddy Crossley (Corporate Finance)
James Stearns (Corporate Broking)
Telefon: +44 207 886 2500
Sisu Partners Oy, Certified Adviser på Nasdaq First North
Juha Karttunen, Jussi Majamaa
Telefon: +358 (0)40 555 4727
Consilium Strategic Communications
Mary-Jane Elliott, David Daley, Lindsey Neville
Telefon: +44 (0)20 3709 5700
E-post: faron@consilium-comms.com
Om MATINS-studien
MATINS-studien är den första öppna Fas I/II kliniska studien på människa med en adaptiv design för att undersöka säkerheten och effektiviteten av Clevegen i utvalda metastaserade eller inoperabla solida tumörer. De utvalda tumörerna som undersöks är kutant melanom, hepatobiliär/hepatocellulär, pankreas-, äggstocks- och kolorektal cancer, som alla är kända för att hysa ett betydande antal Clever-1 positiva tumörassocierade makrofager (TAM). Sammanlagt utgör dessa fem målgrupper cirka 2 miljoner årliga fall globalt. Cancerpatienter med högt Clever-1-uttryck identifieras med en enkel blodmyeloidcellsfärgning med Clevegen (“flytande biopsi”).
Del I av studien behandlar tolerabilitet, säkerhet och dosökning för att optimera dosering. Eftersom studien är en öppen studie förväntar sig företaget att rapportera fynd när doseringen fortskrider. Kohortexpansionen under del II kommer att fokusera på identifiering av patienter som visar ett ökat antal Clever-1 positiva cirkulerande monocyter och säkerheten och effektiviteten av behandlingen. Kolorektal cancer och äggstockscancer har valts som de första och andra expansionskohorterna i del II. Under del III kommer huvudfokus att ligga på att bedöma effekten av Clevegen på studieobjekt som visar ett ökat antal Clever-1 positiva cirkulerande monocyter, vilket gör behandlingen precist riktad och maximerar chanserna till framgång för effekten. Behandlingen, om den är framgångsrik, kan slutligen användas som en fristående terapi eller i kombination med andra immunterapier som PD-1-hämmare.