Hansa Biopharma tillkännager positiva fullständiga resultat från fas 2-studien 15-HMedIdeS-09 och jämförande analys av imlifidase hos patienter med Guillain-Barrés syndrom
Lund, Sverige, 17 december 2024. Hansa Biopharma, ”Hansa” (Nasdaq Stockholm: HNSA), tillkännagav idag positiva fullständiga resultat från den enarmade fas 2-studien 15-HMedIdeS-09 med imlifidase, ett först i klassen IgG-klyvande enzym, vid Guillain-Barrés syndrom (GBS) samt en indirekt behandlingsjämförelse av data från 15-HMedIdeS-09-studien med International Guillain-Barré Syndrome Outcome Study (IGOS), en världsomspännande prospektiv studie av Inflammatory Neuropathy Consortium om prognos och biomarkörer för GBS.
Data från 15-HMedIdeS-09-studien visade att svårt sjuka GBS-patienter som behandlades med en engångsdos imlifidase (0,25 mg/kg) plus intravenöst immunglobulin (IVIg) uppvisade en snabb övergripande förbättring av funktionell status, inklusive påskyndad återhämtning av muskelstyrka, snabb återgång till att gå självständigt, och en mediantid till att gå självständigt (t.ex. att uppnå Guillain-Barrés syndroms funktionsskala (GBS DS) 2 eller mindre) på 16 dagar.
Den indirekta behandlingsjämförelsen drog slutsatsen att patienter i 15-HMedIdeS-09-studien som behandlades med imlifidase plus IVIg återgick till att gå självständigt 6 veckor snabbare jämfört med svårt sjuka GBS-patienter i IGOS-jämförelsegruppen från verkliga världen som behandlades med IVIg. Dessutom upplevde patienter i 15-HMedIdeS-09-studien en statistiskt signifikant förbättring över flera kliniskt meningsfulla mått vid flera tidpunkter jämfört med IGOS-jämförelsegruppen från verkliga världen, inklusive 6,4 gånger större sannolikhet vid vecka 1 och 4,2 gånger större sannolikhet vid vecka 4 att gå självständigt.
Hitto Kaufmann, forsknings- och utvecklingschef, Hansa Biopharma, kommenterade: ”Våra fas 2-studieresultat och den indirekta behandlingsjämförelsen med IGOS är avgörande viktiga. Tillsammans visar de den betydande roll imlifidase kan spela i framtida behandlingsalternativ för GBS-patienter. Till skillnad från andra molekyler kan imlifidase effektivt och mycket snabbt avlägsna IgG genom enzymatisk klyvning – vilket stoppar progressionen av nervskador associerade med GBS och stoppar sjukdomsprogressionen. Huvudmålet med förbättrade GBS-behandlingar är att stoppa nervskador tidigt, minska sjukhustiden och stödja patienter att återfå självständighet snabbare. Dessa fynd understryker den roll patogent IgG spelar i svårighetsgraden och progressionen av GBS, och imlifidases tydliga potential att möta obehandlat behov vid IgG-drivna autoimmuna sjukdomar där snabbare verkande behandlingsalternativ behövs.”
Vid GBS är IgG en nyckelfaktor för inflammatoriska attacker på perifera nerver och har kliniskt kopplats till sjukdomens svårighetsgrad och progression. En snabb minskning av IgG-nivåerna har potential att gynna GBS-patienter genom att utarma patologiska IgG-antikroppar, vilket därmed stoppar sjukdomsprogressionen och resulterar i snabbare återhämtning och mindre allvarlig sjukdom.1 Förbättring av GBS DS är viktigt eftersom det direkt påverkar de kliniska resultaten, återhämtningen och livskvaliteten för patienter. Bättre hantering av sjukdomens svårighetsgrad kan bidra till att minska risken för livshotande komplikationer, förkorta återhämtningstiden, förhindra långvarig funktionsnedsättning, sänka sjukvårdskostnaderna och förbättra patienternas övergripande välbefinnande.
Professor Shahram Attarian, chef för avdelningen för neuromuskulära sjukdomar och ALS, Hopitaux Universitaires de Marseille (APHM), och internationell koordinerande huvudprövare i 15-HMedIdeS-09 fas 2-studien, sade: ”Vid behandling av GBS och den efterföljande återhämtningsprocessen är tidig förbättring och förmågan att gå självständigt viktiga kliniska milstolpar eftersom de indikerar en återgång till grundläggande rörlighet och självständighet, samt till en förbättrad livskvalitet för patienter. Denna analys stöder imlifidases potentiella roll, följt av standardbehandling med IVIg, som ett potentiellt nytt behandlingsalternativ vid GBS. Detta är viktiga resultat för patienter och kliniker inom GBS-gemenskapen.”
Nyckelresultat: 15-HMedIdeS-09-studien
15-HMedIdeS-09-studien inkluderade 30 vuxna patienter som behandlades med imlifidase plus IVIg. Under studien omdiagnostiserades tre patienter, och de återstående 27 patienterna fick en bekräftande diagnos av svår GBS och inkluderades i effektivitetsanalysen.
Vid den första veckan kunde 37 % av patienterna i 15-HMedIdeS-09-studien gå självständigt och den genomsnittliga förbättringen av muskelstyrkan var 10,7 poäng bedömt med Medical Research Council (MRC) sum score.
Mediantiden för att förbättras med minst en grad på GBS DS var sex dagar. Vid åtta veckor kunde 67 % av patienterna gå självständigt, 40,7 % av patienterna hade återfått förmågan att springa, och 37 % av patienterna hade förbättrats med minst tre poäng på GBS DS. Sex månader efter imlifidase-behandling kunde 63 % av patienterna springa eller hade ingen funktionell funktionsnedsättning (GBS DS ≤1). Administrering av imlifidase tolererades väl i studien.
Nyckelresultat: Indirekt behandlingsjämförelse av 15-HMedIdeS-09-studien med jämförelsegruppen från verkliga världen
Jämfört med IGOS-jämförelsegruppen från verkliga världen (svårt sjuka GBS-patienter behandlade med IVIg, n=754), upplevde patienter i 15-HMedIdeS-09-studien (svårt sjuka GBS-patienter behandlade med imlifidase i kombination med IVIg, n=27) en signifikant snabbare förbättring av funktionsnedsättning mätt med GBS DS.
Patienter i 15-HMedIdeS-09-studien förbättrades med minst ett steg på GBS DS, 3 veckor snabbare (p=0,002) och återgick till att gå självständigt (GBS DS≤2) 6 veckor snabbare jämfört med patienter i IGOS-jämförelsegruppen från verkliga världen som behandlades med IVIg (p=0,03).
Dessutom var patienter i 15-HMedIdeS-09-studien mer benägna att snabbt återfå förmågan att gå självständigt än IGOS-jämförelsegruppen från verkliga världen som behandlades med IVIg. Vid en vecka var patienter i 15-HMedIdeS-09-studien 6,4 gånger mer sannolika (odds ratio 95 % konfidensintervall: 2,3-17,5, p<0,001), och vid fyra veckor, 4,2 gånger mer sannolika (odds ratio 95 % konfidensintervall: 1,6-11,5, p=0,005) att gå självständigt än de patienter i IGOS-jämförelsegruppen från verkliga världen som behandlades med IVIg. Resultaten matchades och viktades för olika prognostiska faktorer inklusive tid från svaghetsdebut till behandlingsstart och baslinjevärde för ålder, autonom dysfunktion, kranialnervspåverkan, GBS DS och MRC sum score.
Hansa utvecklar nya immunmodulerande biologiska terapier baserade på sin egenutvecklade, först i klassen IgG-klyvande plattform och fokuserar på IgG-drivna immunmedierade sjukdomar där det finns ett stort obehandlat medicinskt behov och få eller inga behandlingsalternativ. Företaget har två IgG-klyvande föreningar. Imlifidase är en första generationens, först i klassen, engångsdosbehandling med bevisad effekt och säkerhet. Den är villkorligt godkänd i EU för desensibilisering vid njurtransplantation. HNSA-5487 är en andra generationens molekyl med potential för upprepad dosering med en klinisk utvecklingsväg fokuserad på akuta exacerbationer vid neuroautoimmuna sjukdomar inklusive myasthenia gravis (MG).
Företaget planerar att publicera data från studien och den indirekta jämförelsen. Mer information om studien finns på ClinicalTrials.gov under NCT03943589.
Hansa Biopharma kommer att hålla en telefonkonferens den 18 december kl. 14:00 CET / 8:00 AM ET.
Presentationsbilder kommer att finnas tillgängliga online efter samtalet.
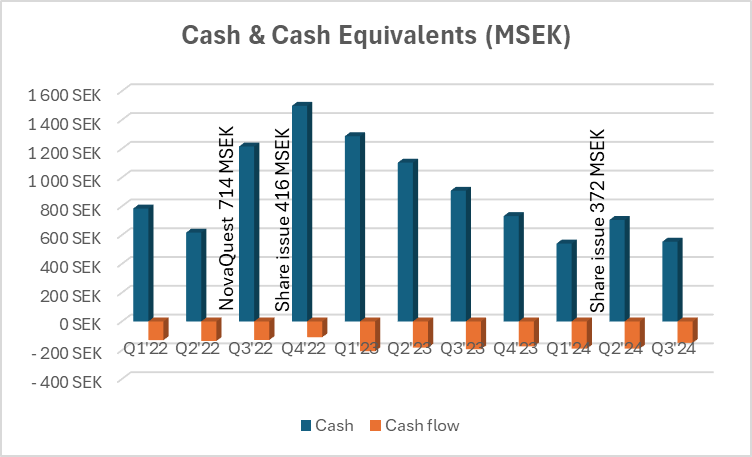
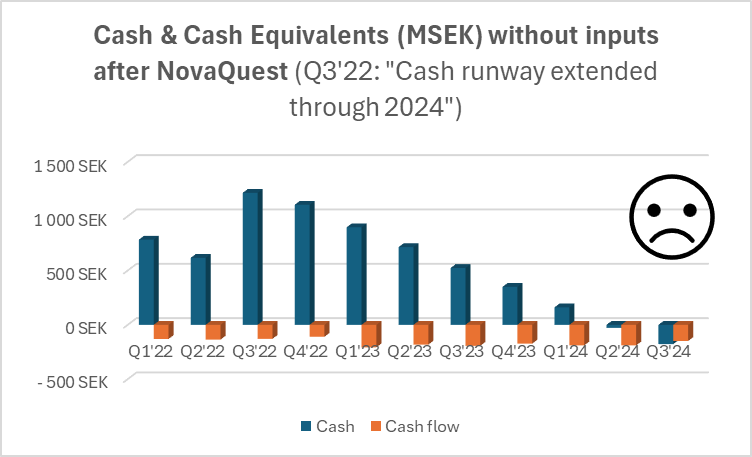
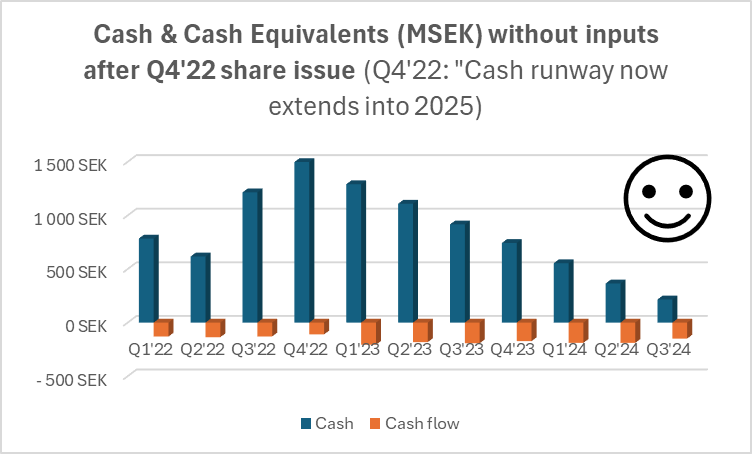
![]() ), har Hansa varit ganska proaktiv i sina finansieringsarrangemang, vilket enbart är positivt. Farons krisemission i våras genomfördes å andra sidan på ett småspararvänligt sätt, medan Hansa har fokuserat på riktade emissioner. Den senaste var förstås till marknadspris, vilket tackas för från småspararhåll
), har Hansa varit ganska proaktiv i sina finansieringsarrangemang, vilket enbart är positivt. Farons krisemission i våras genomfördes å andra sidan på ett småspararvänligt sätt, medan Hansa har fokuserat på riktade emissioner. Den senaste var förstås till marknadspris, vilket tackas för från småspararhåll ![]() .
.