Maijalla on kyllä merkittävä vaikutus. Juhohan jossakin haastatteluissa (olikohan S. Miettisen?) totesi, että Maijaa on tarvittu neuvotteluissa vääntämään tiedeasioita rautalangasta vastapuolelle. Helppo ajatella, että kaikkien epäonnisten makrofagilääkkeiden jälkeen BP:n ensireaktio on ”iik, makrofagi, iik CD47, good bye 4,9 BUSD”. Mutta ehkä this time is different? Ilman toista kovaa tiedemuijaa, Sirpaa, ei myöskään Faronia olisi ainakaan Bex-mielessä.
Maijalla on jalat maassa, Turun Sanomissa 10/23 ”Täytyy oikein ihmetellä sitä, kuinka hyvät vasteet sillä on ollut, sanoo syöpäimmunologian dosentti Maija Hollmén hymy huulillaan.– Se ei ole ihmelääke, mutta se on tavattoman mielenkiintoinen”. Mitähän hän nyt 2 vuoden jälkeen toteaisi?
Yhteenveto
Bexmarilimab ja makrofagien uudelleenohjelmointi
”Olen erittäin iloinen saadessani olla täällä kertomassa siitä, mitä teemme yliopistolla ja Faron Pharmaceuticalsilla. Kuten mainittiin, toimin Faronin tieteellisenä johtajana (CSO), mutta minulla on myös akateeminen laboratorio Turun yliopistossa. Kuulumme InFLAMES-lippulaivahankkeeseen, jota Suomen Akatemia rahoittaa ja jossa teemme tutkimusta immuniteetista ja siitä, kuinka immuunisoluja voidaan hyödyntää hoidollisesti.
Puhun teille tutkimuksestamme makrofagien uudelleenohjelmoinnista hoidollisia hyötyjä varten. Olemme työskennelleet tämän parissa laboratoriossani ja yhteistyökumppaneiden kanssa jo vuosia. Olen iloinen, että Andrea on jo kertonut teille paljon makrofageista, joten en mene syvällisiin yksityiskohtiin kasvaimeen liittyvistä makrofageista (TAM). Ne ovat kuitenkin erittäin monipuolisia soluja ja tekevät monia asioita edistääkseen kasvaimen etenemistä ja etäpesäkkeiden muodostumista.
Lähestymistapani makrofagien uudelleenohjelmointiin – jotta saisimme aktivoitua luontaisen (innate) ja hankinnaisen (adaptive) immuunivasteen – perustuu niiden toimintaan scavenger-reseptoreiden (puhdistusreseptoreiden) kautta. Nämä reseptorit keräävät kasvainympäristöstä erilaisia komponentteja, jotka edistävät makrofagien toleranssia ja tukevat kasvaimen kasvua. On olemassa myös muita komponentteja, joita voidaan stimuloida agonistisilla vasta-aineilla kasvainvastaisten vaikutusten aikaansaamiseksi, mutta puhun pääasiassa scavenger-reseptoreista, koska olemme tutkineet niitä.
Pääpointti on, että estämällä scavenger-reseptoreita (tai muita reseptoreita, jotka vaikuttavat tolerogeeniseen makrofagifenotyyppiin) tai aktivoimalla kasvainvastaisia kohdemolekyylejä, voisimme lisätä antigeenien esittelyä kasvaimeen liittyvissä makrofageissa. Tämän jälkeen voisimme houkutella paikalle CD8-positiivisia T-soluja ja NK-soluja sekä käynnistää syöpäsolujen tappamisen ja fagosytoosin.
Teimme tohtorikoulutettavani kanssa vuonna 2024 systemaattisen katsausartikkelin, koska halusimme ymmärtää makrofagien uudelleenohjelmointihoitojen kliinistä maisemaa. Kävimme läpi yli 700 tutkimusta ja lähes 200 eri lääkekohdemolekyyliä. Tutkimus on laajentunut merkittävästi vuodesta 2010. Merkittävin kohde alalla on CD47-SIRPa-akseli, josta on paljon kliinisiä kokeita, mutta mukana on myös Toll-like-reseptoriagonisteja, LILRB-reitti ja IDO1. Kovin monia onnistuneita kokeita ei kuitenkaan ole ollut. Makrofagien uudelleenohjelmointihoidot eivät yleensä toimi hyvin monoterapiana; T-solujen täytyy aktivoitua. Lisäksi on monia rinnakkaisia reittejä: jos estät yhtä, toinen aktivoituu. Siksi esimerkiksi pelkkä IDO1:n esto ei ole kovin tehokasta. Oli mielenkiintoista huomata, että 6 000 potilasta hoidettiin IDO1-estäjällä ennen kuin kehitys lopetettiin. CD47-eston ympärillä on myös paljon yrityksiä, mutta näillä hoidoilla on sivuvaikutuksia, mikä on johtanut joidenkin kokeiden keskeyttämiseen.
Clever-1 ja Bexmarilimab
Me olemme työskennelleet Clever-1:n parissa. Se on scavenger-reseptori, jota ilmentyy makrofageissa ja endoteelisoluissa. Nimi tulee sanoista Common Lymphatic Endothelial and Vascular Endothelial Receptor, mutta se tunnetaan myös nimillä Stabilin-1 ja FEEL-1. Makrofageissa Clever-1-ilmentyminen säätelee toleranssia, lievittää tulehdusta ja aiheuttaa immunosuppressiota kudoksissa, mutta säätelee myös kudoksen homeostaasia puhdistamalla bakteereja ja apoptoottisia soluja. Endoteelipuolella se säätelee liikennettä. Turun yliopiston alkuperäisessä tutkimuksessa havaittiin, että Clever-1 säätelee myös syöpäsolujen etäpesäkkeiden leviämistä imusolmukkeisiin.
Kun estämme Clever-1:tä, kasvainten kasvu ja etäpesäkkeiden muodostuminen vähenevät. Käytimme poistogeenisiä (knockout) hiiriä ymmärtääksemme mekanismia. Kun istutimme Lewis-keuhkokarsinoomasoluja (Lewis Lung Carcinoma) tai kolmoisnegatiivisia rintasyöpäsoluja hiiriin, joilta Clever-1 puuttui vain myelooisista soluista, kasvaimia ei kasvanut lainkaan. Kasvaimet olivat täynnä CD3-positiivisia T-soluja, erityisesti CD8-sytotoksisia T-soluja.
Hieman historiaa: Alun perin Sirpa Jalkanen Turun yliopistossa tutki molekyylejä selvittääkseen, miten lymfosyytit kulkevat imusolmukkeisiin. Hän löysi vasta-aineen nimeltä 3-372, joka värjäsi imusuonten endoteelisoluja, ja Heikki Irjala nimesi molekyylin Clever-1:ksi. Samaan aikaan ryhmät Japanista ja Saksasta löysivät saman molekyylin (FEEL-1 / Stabilin-1).
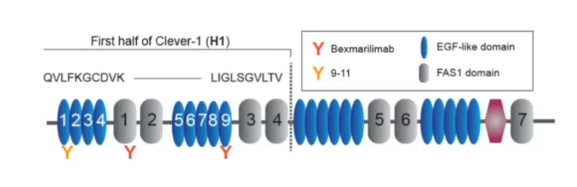
Miten päädyimme lääkekehitykseen? Vuonna 2003 tunnistettiin Clever-1:n rooli syöpäsolujen sitoutumisessa. Vuonna 2007 perustettiin Faron Pharmaceuticals. Alkuperäinen hiiren vasta-aine (3-372) humanisoitiin ja muutettiin IgG4-muotoon – näin syntyi bexmarilimab. Siihen tehtiin kaksi pistemutaatiota: ensimmäinen estämään Fab-varsien vaihtumista (mikä on tyypillistä IgG4:lle) ja toinen vaimentamaan efektoritoimintoja (kuten ADCC), jotta vältettäisiin toksisuus endoteelisoluja kohtaan.
Mekanismi on seuraava: Normaalisti Clever-1 kerää ”roskaa” (kuten asetyloitua LDL:ää), mikä edistää makrofagin toleranssia ja IL-10:n tuotantoa. Kun annamme bexmarilimabia, se sitoutuu Clever-1:een ja estää sen toiminnan. Se myös estää endosomien happamoitumisen (sitoutumalla V-ATP-aasiin), mikä vaikuttaa antigeenien prosessointiin ja esittelyyn. Tämä johtaa MHC-molekyylien ja antigeenien parempaan esittelyyn sekä tulehdussytokiinien (kuten CXCL10, CCL5) tuotantoon.
Kliiniset tulokset (MATINS-tutkimus)
Ensimmäinen ihmisillä tehty tutkimus oli nimeltään MATINS. Se oli “kori-tutkimus” (basket trial), jossa tutkittiin 10 eri kasvaintyyppiä levinneessä vaiheessa olevilla potilailla. Tämä oli monoterapia-tutkimus. Havaitsimme, että bexmarilimab oli hyvin siedetty ja saavutimme taudin hallinnan (disease control) myöhäisen vaiheen syövässä. Rintasyövässä näimme 35–40 % taudin hallinnan.
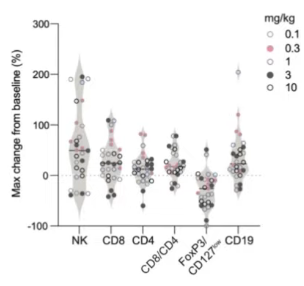
Biopsianäytteistä näimme, että vasteen saaneilla potilailla kasvaimeen liittyvät makrofagit (TAM) aktivoituivat, mikä johti korkeampaan interferoni-gamma-tasoon verenkierrossa. Mielenkiintoista oli, että matala lähtötason immuuniaktivaatio ennusti hyötyä bexmarilimabista. Verenkierrossa näimme NK-solujen, CD8- ja CD4-T-solujen sekä B-solujen voimakkaan lisääntymisen, kun taas säätelijä-T-solujen (Treg) määrä väheni.
Soluble Clever-1 (Liukoinen Clever-1)
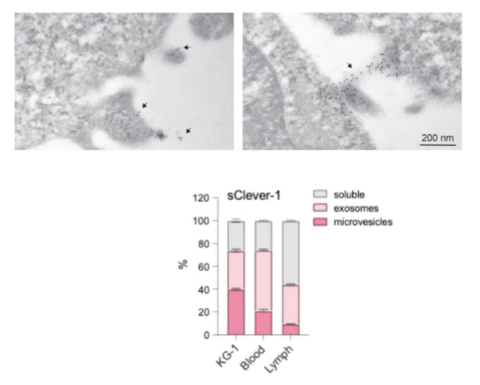
Olemme havainneet, että makrofagit ja endoteelisolut voivat erittää Clever-1:tä solunulkoisissa rakkuloissa tai liukoisessa muodossa. Syöpäpotilailla (erityisesti rintasyöpä) on plasmassa enemmän liukoista Clever-1:tä kuin terveillä. Bexmarilimab-hoito vähensi näitä tasoja merkittävästi.
Selvitimme, että liukoinen Clever-1 (erityisesti sen H1-fragmentti) sitoutuu aktivoituihin T-soluihin (CD8+ PD1+ muistisoluihin). Tämä sitoutuminen tapahtuu immunologisen synapsin aikana. Se sitoutuu IGF2R-reseptoriin (Insulin-like Growth Factor 2 Receptor), estää LCK:n fosforylaation ja lisää FoxP3-positiivisten säätelijä-T-solujen määrää. Käytännössä liukoinen Clever-1 toimii “liukoisena tarkastuspisteenä” (soluble checkpoint), joka hillitsee immuunivastetta.
Hematologiset syövät (MDS/AML)
Clever-1:tä ilmentyy runsaasti myös myelooisissa syövissä, kuten akuutissa myeloosissa leukemiassa (AML) ja myelodysplastisessa oireyhtymässä (MDS).
Teimme faasin 1/2 tutkimuksen (BEXMAB), jossa bexmarilimabia annettiin yhdessä atsasitidiinin kanssa. Näimme, että yhdistelmä lisäsi antigeenien esittelyä (HLA-DR) ja CD3+ T-solujen määrää luuytimessä. Luuytimen uudelleenmuotoutuminen oli voimakasta: immunosuppressiiviset monosyytit katosivat ja punasolujen sekä verihiutaleiden esiasteet lisääntyivät.
Faasin 2 tulokset osoittivat korkean hoitovasteen MDS-potilailla. Jotkut saivat täydellisen vasteen, ja pystyimme viemään potilaita kantasolusiirtoon. Keskimääräinen elossaoloaika (OS) oli 13,4 kuukautta, mikä on erittäin hyvä tulos tässä potilasryhmässä (normaalisti n. 6 kk). Mitä paremmin bexmarilimab sitoutui liukoiseen Clever-1:een luuytimessä, sitä paremman vasteen potilas sai.
Yhdistelmä atsasitidiinin kanssa toimii synergistisesti: atsasitidiini käynnistää adaptiivisen immuunivasteen, kun taas bexmarilimab herkistää syöpäsolut (blastit) apoptoosille vaikuttamalla mitokondrioihin.
Keskustelu (Q&A)
Kysymys: Mikä on annosteluaikataulu? Voiko liian tiheä annostelu häiritä immuunijärjestelmän säätelyä?
Vastaus: Kiinteiden kasvainten tutkimuksissa annoimme lääkettä joka kolmas viikko. Vaikka vasta-aine poistuu nopeasti, farmakodynaamiset vaikutukset kestävät pidempään. Emme usko, että aiheutamme liiallista tulehdusvastetta. Kyse on enemmänkin immuunijärjestelmän “buustaamisesta”. Hematologisissa syövissä annostelu on viikoittaista, jotta saamme pidettyä kohteet (blastisolut) sitoutuneina.
Kysymys: Onko suunnitelmissa yhdistää bexmarilimab anti-PD-1-hoitoon?
Vastaus: Kyllä. Hiirikokeet viittaavat siihen, että yhdistelmällä on additiivinen vaikutus kasvaimissa, jotka eivät reagoi pelkkään PD-1-estoon. Olemme aloittamassa tutkimusta tästä.
Kysymys: Missä näet tämän 10 vuoden päästä? Voiko tämä tulla ensilinjan hoidoksi?
Vastaus: Toivomme niin. Hematologisissa syövissä olimme jo ensilinjassa (hoitamattomat potilaat). Rintasyövässä olemme siirtymässä aikaisempiin hoitolinjoihin. Tärkeää on ymmärtää, että lääkkeemme vaatii toimivan adaptiivisen immuunijärjestelmän. Jos potilaan luuydin on täysin uupunut hoidoista, lääkkeemme ei toimi.
Kysymys (Mac4Me-projektista): Mitä suosittelisit väitöskirjatutkijoille?
Vastaus: Käyttäkää malleja, joilla on translationaalista (siirrettävää) arvoa. Minun laboratoriossani tehdään harvoin hiirikokeita enää; pyrimme käyttämään ihmisperäisiä malleja ja primäärisoluja, jotta tulokset olisivat todenmukaisia. Käyttäkää oikeita malleja oikeisiin kysymyksiin.
Kysymys: Vaikuttaako ikääntyminen vasteeseen?
Vastaus: Emme tutkineet tätä hiirillä, mutta ihmisillä liukoisen Clever-1:n määrä kasvaa iän myötä. Syöpä on suurin syy nousuun, mutta ikä on seuraava. Hiiri ei välttämättä ole paras malli Clever-1:lle, koska hiiren monosyytit eivät ilmennä sitä yhtä paljon kuin ihmisen.”
Ehkä Maija ei ole ihmeidentekijä, mutta ainakin hän on tavattoman mielenkiintoinen. Tai kohtahan ne ihmeet ilmenevät, jos…