Faron aikoo mennä FDA pakeille faasi 2b tulosten tiimoilta ja kuten juuri kuultiin, CR ja sen kesto on se, mitä tavoitellaan. Aiheesta yksi tutkimus; portaalista klikkaa Zeidanin Bex-esityksen alta Julie, kuuluu siihen ASH-pakettiin, joka aiheutti Tänka På:n.
https://www.vjhemonc.com/event/post-ash-2025-mds-highlights/
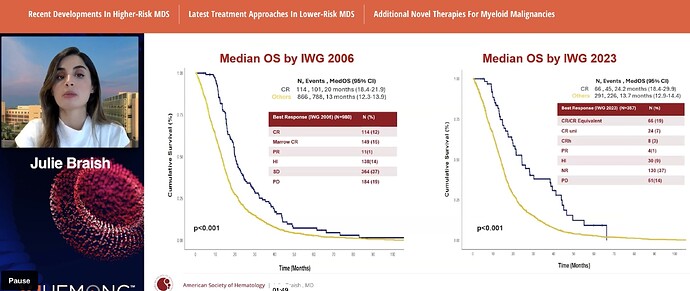
”Durability of complete response outperforms complete response rates as a surrogate endpoint for advancing to phase III trials in high-risk myelodysplastic syndromes”
Julie Braish University of Texas MD Anderson Cancer Center, Houston, TX, United States
Moffitt Cancer Centerissä tehty tutkimus, taaksepäin katsova eli hoidon jälkeen kerätty tiedot, 980 potilasta HR-MDS (intermediate ja vaikeammat).
Selvittelyä, miksi menestys faasi 1/2:ssa ei siirry faasi 3:een, joka aiheena on nyt kuuminta hottia, kuten tiedetään… Erityisesti TP53 ongelmallinen. Siinä CR kyllä nähdään, mutta lyhyinä.
Hypoteesi: CR, joka on kestoltaan 6 kk tai yli ennustaa paremmin elinaikahyötyä eli OS, kuin pelkkä CR kerran saavutettuna vasteena.
Luuydinsiirtoon meneviä ei otettu analyysiin mukaan. (Siirrot on suunnitelmassa käsiteltävä niin, että eivät rankaise Bexiä, jos CR kesto katkaistaan toivottuun siirtoon mennessä toim. huom.)
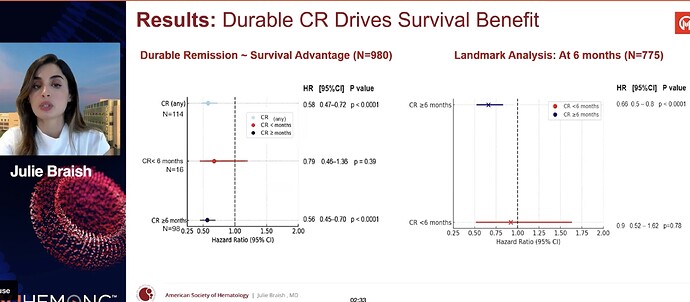
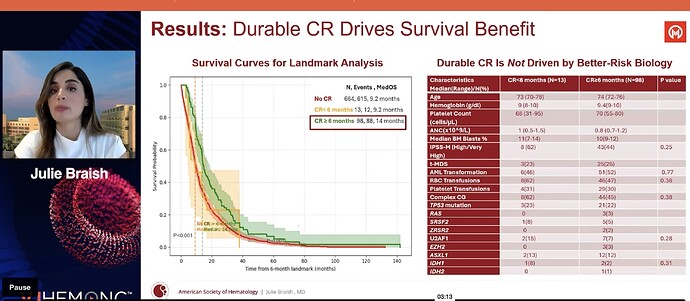
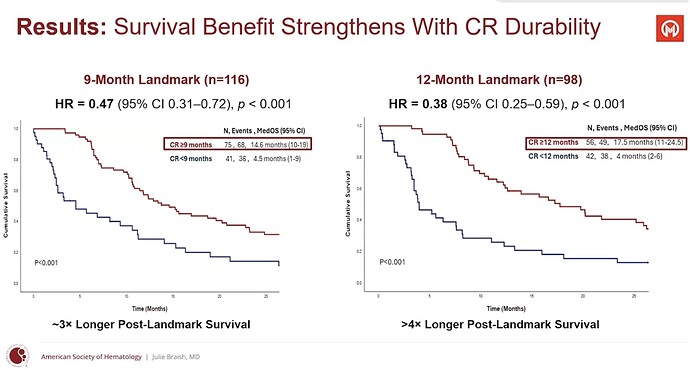
Osoittivat, että mitä pitempi CR, sitä pitempi survival (aika obvious). CR sinänsä myös toimii. Surrogaattina eli elinaikahyötyä ennustavana tekijänä heidän mielestä (sellaisena, joka FDA:n hyväksymänä voisi tarkoittaa AA-myyntilupaa toim. huom.) voisi pitää CR kestoa 6 kk tai yli. Nythän CR jo on sellainen ollut. Mikä riittää ensi vuonna FDA:lle, ei ole tiedossa, guidancessa vain sana ”meaningful”.
Mitä Faron kertoo noista vasteiden kestoista?
liiketoimintapäivitys | 11. helmikuuta 2026 Faron Pharmaceuticals - Innovatiivisia lääketieteen ratkaisuja (Osa 2) - #3416 käyttäjältä Vino_Pino :
”Seuranta on vielä kypsymätön (käsittääkseni oli marraskuun luenta toim. huom.), mutta CR:n mediaanikesto on jo yli 12 kuukautta, ja seuranta jatkuu – mahdollisesti se vielä nousee. TP53-mutatoituneilla potilailla CR-prosentti oli hämmästyttävä 70 prosenttia, ja CR:n kesto taas yli 10 kuukautta, mahdollisesti edelleen nouseva. Historiallisesti tämä potilasryhmä elää yleensä 8–10 kuukautta.”
Noita lukuja katsoen näyttää, että aletaan olla turvallisella alueella. Uudet lukemat varmaan kuukauden päästä BSH:ssa. Mediaani yli 12 kk tarkoittaa, että vähintään puolella potilaista vasteet ovat kestäneet yli 12 kk. Moffittin tutkimuksessa 6 kk raja on sen sijaan vasteen keston vähimmäisaika, joka pitäisi jokaisen ylittää.
Voi olla, että ”aina” faasi 1/2a:han valikoidaan helpot potilaat ja satunnaistetuissa vasta totuus ja arki valkenee. Nyt voi olla toisinkin päin, jos/kun on valikoitu TP53 potilaita enemmän kuin heidän luonnollinen osuutensa olisi. Jos alustavat havainnot siitä, että soluvajeita tulee vähemmän Bexin kanssa kuin ilman, faasi 3 koetut ongelmat osin kääntyvätkin Bexin eduksi, koska ei tule vaarallisia vajeita, kuten monella muulla toksisella. No, faasi 2b/3 vasta näyttää, miten käy.
Tuleepahan se ”montako sykliä” on saatu azaa vaikuttavana seikkana myös kontrolloitua. Viitettä faasi 2b tulevasta menestyksestä voidaan saada, jos näitä CR-kesto-surrogaatteja syynätään.
R/r potilaiden tutkiminen lopulta avasi nyt aivan uuden tien eteenpäin, City of Hopen jatkon, IIT:n, saa nähdä tarvitseeko minkälaisen tuen faasi 2b:stä vai mitä siellä ajatellaan kommunikaatiosta regulaattorin kanssa