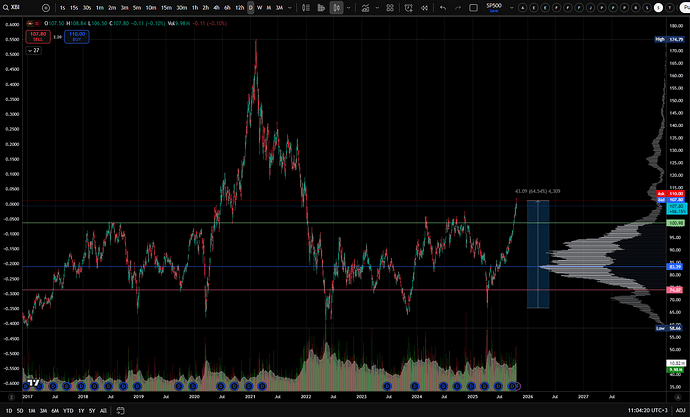
Kirjoittelen alla yleisesti biotechien markkinatilanteesta. XBI eli (SPDR S&P Biotech ETF) on tällä hetkellä yksi jenkkimarkkinoiden parhaiten suorituvista sektoreista. Tilanne oli lähes päinvastainen vielä keväällä, kun FDA oli mylleryksessä Trumpin astuttua valtaan, korot olivat korkealla, koronlaskuodotukset epäselvät ja kauppasodan huolet pinnalla. Lisäksi alkuvuonna useampi kliininen tutkimus epäonnistu, regulaatiopuolelta tuli takapakkia ja ilmapiiri oli epäselvä.
Syitä XBI:n n. +60% nousulle pohjilta voi hakea mm. koronlaskuista ja FED:n QT:n todennäköisestä päättymisestä, jotka keventävät rahoitusolosuhteita mm. riskisten sijoitusten osalta. Myös M&A on ollut nousussa ja Big Pharma metsästää taas innovatiivisia diilejä mm. syöpä- ja alzheimerlääkekehityksen sektorilta. Lisäksi väestön ikääntyminen ja lisääntyvät terveyssektorin panostukset helpottavat rahoitusta hakevien startuppien tilannetta, johon vaikuttavat positiivisesti myös useiden patenttien vanheneminen lähivuosien aikana.
Vaikka rahoitustilanne ei ole niin hyvä kuin vuosina 2020-21, niin lääkefirmoilla on investointitarpeita ja rahoitusolojen keventyessä sekä korkotason stabiloituessa näkisin investointitahdin olevan taas selkeästi nousujohteisempaa, kuin muutama kuukausi takaperin.
Mm. onkologian ja harvinaisten sairauksien puolelta on nähty tänä vuonna useita onnistumisia, kuten keuhkosairauksissa Zongertinib ja Sunvozertinib, rintasyövissä Inluriyo (imlunestrant), harvinaisten syöpäsairauksien puolelta Penpulimab ja Belzutifan, aivo- pää ja niskasyöpien puolelta Dordaviprone sekä Perioperative pembrolizumab ja virtsarakkosyövistä Inlexzo (gemcitabine intravesical system). Kaiken kaikkiaan FDA oli myöntänyt syyskuuhun mennessä yhteensä 30 hyväksyntää onkologian puolelta.
Lisäksi harvinaisten sairauksien osalta tämän vuoden aikana on hyväksytty Forzinity (elamipretide), sekä viime vuonna Ctexli (chenodiol), Hympavzi (marstacimab) ja Miplyffa (arimoclomol).
FDA on myös alkanut hyväksymään entistä enemmän AA:ta (accelerated approval) mm. geeniterapioissa ja harvinaisemmissa sairauksissa. Mielestäni Faron on aika lailla odottamassani aikataulussa ja Juhon sanojen mukaan palapelin palaset alkavat olla viimein kasassa. Edellä mainittuihin taustoihin peilaten myös Faronin phase 3 rahoitustilanne alkaa näyttämään aiempaa paremmalta, varsinkin FDA:n hyväksymisprosessien selkeydyttyä ja rahoitusolojen keventymisen seurauksena.
Bonon mietteet ja kuvia esityksestä. Itseä hymyilytti toisen kuvan panelistien ilmeet, ketä lie ovatkaan. En ole varma mitä ajattelivat, olivatko mykistävät tulokset hyviä vai huonoja ilmeistä päätellen ![]()
Edit: oli jostain syystä väärä linkki ja kuvat
Mutta missä on herra tietäjä VinoPino ? Olisi mukavaa kuulla hänen mietteitä sekä analyyseja tilaanteesta Faron ![]()
![]()
Harmi ettei saatu isompaa nousua CR lukemaan, vaikka 45% onkin jo hyvin vaikuttava. Nyt tosin nousu johtui siitä, että n oli pienentynyt yhdellä (21 >> 20).
edit: Toki jos olen oikein ymmärtänyt, CR lukemasta puuttuvat IWG2006 kriteeristöllä ne, joilla alun perinkin BM blasteja <5% ?
Onko näin?
”The most significant update is the new pharmacodynamic data that provided a clear biological explanation for the strong clinical results. The analysis showed a statistically significant correlation (p=0.0006) between deeper engagement of the Clever-1 target in the bone marrow and a positive clinical response. This correlation was particularly striking in the subgroup of treatment-naïve patients with <5% bone marrow blasts at baseline (38% of the cohort), a population for which effective, non-intensive therapies are urgently needed. In these patients, deeper target engagement translated to a 100% ORR, supporting bexmarilimab’s unique mechanism of action as a truly disease modifying agent, differentiating it from other investigational HR-MDS therapies, such as Bcl-2 inhibitors. For patients with a higher blast count (>5% at baseline), the ORR remained high at 75%.”
38 % saisi kokonaisluvun 8 (7,98) jos se lasketaan 21 potilaasta. CR% 45 sisältää 9/20 potilasta.
Eli onko maksimi CR voinut olla vain 13 / 20 x 100 = 65 %, koska kahdeksaa ei ole voitu laskea mukaan?
Eli voiko laskea myös, että CR on ollut 45 / 65 x 100 = 69 %?
Tai yksinkertaisemmin 9 / 13 x 100 = 69 %
Eli kaikki menee nimittäjään, mutta vain kelvolliset osoittajaan, mutta sitten jos siivotaan epäkelvot pois, niin CR% onkin paljon korkeampi.
EDIT: Vähän sekava viesti ehkä. Mutta siis tuossa potilasryhmässä olisi vain 13 potilasta joille voidaan CR laskea ja näistä 9 on sen saavuttanut.
EDIT2: Korjasin laskelmia. Ei oo helppo homma puhelimella, tällä alustalla jos on %-merkkejä mukana.
Joo ei se taida ihan noin olla kuin luulin. Täällä avattu IWG2023 kriteeristöä: Consensus proposal for revised International Working Group 2023 response criteria for higher-risk myelodysplastic syndromes | Blood | American Society of Hematology
Eli IWG2006 kriteereillä nämä joilla baseline BM blasts <5% voivat saavuttaa CR:n, mutta IWG2023 raportoitaisiin CReq. Käy hyvin ilmi myös kyseisen sivun Table 4 case 6:sta.
Tässä on Antin kommentit tuoreista tutkimustuloksista. ![]()
Faron tiedotti maanantaina uusista tutkimustuloksista, joita esiteltiin viikonloppuna ESMO-kokouksessa. Yhtiön BEXMAB-tutkimuksen päätulokset ovat jo olleet tiedossa, joten nyt kerrotut lisätulokset täydensivät kokonaiskuvaa. Näkemyksemme osakkeesta säilyykin tiedotteen jälkeen ennallaan. Faron järjestää tuloksista torstaina webcastin, jota voi seurata täällä.
Ralphie menossa jutustelemaan mukavia.
Mihinkäs VinoPino ja Clark ovat hävinneet? ![]() Mukava olisi kuulla asiantuntijoiden milipiteitä viimeisimmistä tuloksista.
Mukava olisi kuulla asiantuntijoiden milipiteitä viimeisimmistä tuloksista.
X-kirjoittajan julkaiseman sliden mukaan 12/53, mukana oli ensilinjan potilaita. En vetäisi johtopäätöstä, että beksin käytöllä tässä on ollut merkitystä.
ESMOn slidet löytyy myös Faronin sivuilta:
En nopeasti katsottuna huomannut niitä tänne aiemmin linkatun.
Timo lisännyt 300 000 osakkeen edestä näkemystä ettei antia ole tulossa.
Katsoin kanssa samaa, että Timolta ei vissiin ole tiedusteltu halukkuutta osallistua antiin, joten seurasin Timon jalanjälkiä ja ostin ![]()
Kyllähän tämä on erittäin posi uutinen. Hieman kumminkin paremmin perillä yrityksen asioista Timo kuin me ![]()
Timon lisäyksen myötä oon 95% varma että partneri tulee tänä vuonna. Miks pääomistaja ostais 300 000 osaketta nyky kurssilla jos tulis anti parin kuukauden sisää paljon halvemmalla?
Niinpä.
Kyllä tämä on oikea paikka niille spekulaatioille. Tällaisen firman kyseessä ollen spekulaatioita ei voi välttyä. Ja samaa mieltä, että Timon osto oli kyllä positiivinen signaali ja jos häneltä löytyy luottoa, niin löytyy sitä minultakin.
Ilmoituksen syy (merkitse asianmukainen ruutu tai ruudut “X”:llä)
Rahoitusvälineiden hankinta tai luovutus X
Muu (tarkenna) iii: Muutos johtuen suunnatusta osakeannista (Private Placement) n/a
Analyysistä: “Potilaiden jakautumista ensi- ja toisen linjan potilaiden välille ei kerrottu, mikä vaikeuttaa tuloksen tulkintaa.”
Ymmärsin että frontline on 20 henkilöä ja relapsed (r/r) on 32 henkilöä. Näin ainakin Carnegien rapsassa kerrottiin ![]()
Taudin parantavaan kantasolusiirtoon oli päässyt 23 % kaikista BEXMAB-tutkimuksen potilaista. Potilaiden jakautumista ensi- ja toisen linjan potilaiden välille ei kerrottu, mikä vaikeuttaa tuloksen tulkintaa.
Siis sitä ei kerrottu olivatko kantasolusiirtoon päässeet ensilinjaa vai uusiutuvaa/uppiniskaista syöpää omaavia. Jälkimmäisessä tuo olisi oletettavasti ratkaisevampi apu.