Sen verran on kerrottu, että paastona AUC oli tuolla välillä ja Cmax jäi vähän matalaksi (viime kesänä). En ihan tarkkaan muista kuinka paljon yleisölle jaettiin fed state-tutkimuksesta viime osarin yhteydessä, vilkaisin kyllä mutten ole nyt ihan niin tarkkaan seurannut kun en enää omista. Varmaan kurssi rojahtaa aika kunnolla, kun ensimmäiset kassavirtapositiiviset vuodet tässä taisivat siirtyä ja kassaa ei taida niin pitkällle/varmaan kalliisiin tutkimuksiin ilman lisärahoitusta. Mutta sitten aukeaa tämä jerej:n hehkuttama pitkä peli eli nämä nanoformuloidut subkutaaniin sopivat biologiset lääkkeet, mikä minustakin on vaikuttanut muutenkin kuin patenttikikkailujen kautta lisäarvon luomiselta, ehkä peli aukeaa pitkäksi aikaa ja houkuttelevilta kurssitasoilta?
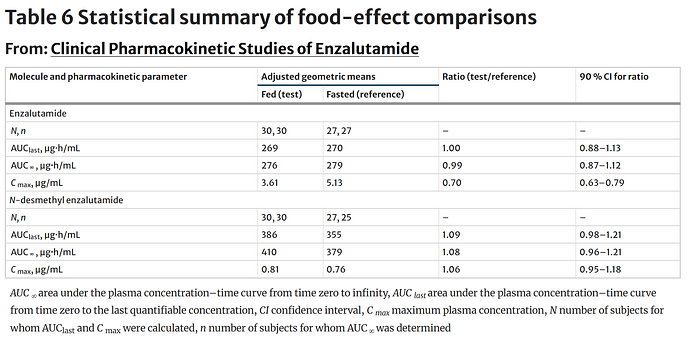
Jaahas, tämmöinen himmeli nyt sitten vastassa. Jääkö se nyt roikkumaan tuon Cmaxin vuoksi? Kaivelin enzalutamidin food effectin dataa täältä. Tässä Cmax laskee fasted ja fed tilojen välillä alle tuon 0.80-1.25 välin.
Lisäksi lainaus artikkelista, lisäsin lihavoinnin.
The geometric mean C max was approximately 30 % lower and median t max was approximately 1 h later with food. The 90 % CI for the ratio of treatment mean C max values was 0.63–0.78, which is below the 0.80–1.25 range to establish absence of a food effect. Taken together, the results show that there was a negligible change in AUC and a slightly lower C max when enzalutamide was taken after a high-fat meal. These C max changes are not considered clinically relevant.
Anyway, nyt kysymyksenä lienee, millaisilla kokeilla tuo hakemus voidaan viedä eteenpäin, miten kauan siihen menee aikaa ja paljon se vaatii rahaa? Miten paljon enzalutamidi projektin eteneminen vaikutaa siihen sidottuihin etappimaksuihin? Nykyinen kassa taitaa riittää noin 2 vuotta tämänhetkisellä poltolla.
Mutta enkö kuitenkin ymmärrä oikein, että nanoentsalutamidin fasted state- Cmaxia verrataan entsalutamiden fasted state- Cmaxiin ja sen pitää olla 80-125% välillä geneeristä hyväksymispolkua varten? Eikä niin, että nanoentsalutamidin paasto- Cmaxin pitäisi olla 80-125% välillä entsalutamidun fed-state arvoon nähden jotta homma voi toimia tämän etenemistavan mukaan?
Nythän sanottiin, että tämä ilmoitus koskee vaan Eurooppaa, muut suunnitelmat eivät ole muuttuneet.
Mutta niistä muista suunnitelmista, varsinkin US, ollaan oltu kovin hiljaa viime aikoina ja keskitytty Euroopan hyväksymispolkuun ja aikatauluun…
Kyllä, näin ainakin itse tuon ymmärrän. Siellä mennään bioekvivalenssin määritelmien mukaan, jolloin noiden kaikkien tulisi olla tuon verrokin arvojen puitteissa. Lähinnä tuossa on hullunkurista se, että tuon korkeamman piikin tulee vastata verrokkia, vaikka sillä tuskin on biologista eroa, jos fed ja fasted kerran toimivat molemmat verrokissa. Nyt lienee tarpeen järjestää isommat kokeet, jotta voidaan näyttää, että tuolla ei ole merkitystä. Se maksaa paljon ja hidastuttaa prosessia, mutta onnistumistodennäköisyys lienee kuitenkin lähes varma tuon kokeen osalta.
Tuo ajan kuluminen taas on huono tuon patentin ikkunan vuoksi. Olisi tärkeä, että nanoenzalutamidi saadaan markkinoille siihen väliin, missä lääkeaineen patentti on rauennut, mutta ASD formulaaation patentti on vielä voimassa. Tuo vähentää kilpailua siinä vaiheesa kun pitää saada merkkinaa vallattua. Josain aiemmassa kvartaaliraportissa johto totesi, että nämä mahdollisesti vaadittavat laajemmat kokeet saataisiin kuitenkin toteutettua vielä ennen tuon 2028 patentin aikarajan loppua, jolloin kaupallistaminen ei myöhästyisi ainakaan suuresti. No, toukokuussa Q1 raportin myötä pitäisi saada viimeistään lisää infoa johdolta, miten tuo prosessi nyt viedään eteenpäin.